Produktnavn:Methylethylketon
Molekylært format:C4H8O
CAS-nr.:78-93-3
Produktets molekylære struktur:
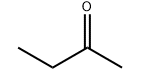
Specifikation:
| Punkt | Enhed | Værdi |
| Renhed | % | 99,8 minutter |
| Farve | APHA | 8max |
| Syreværdi (som acetatsyre) | % | 0,002 maks. |
| fugtighed | % | 0,03 maks. |
| Udseende | - | Farveløs væske |
Kemiske egenskaber:
Methylethylketon er modtagelig for forskellige reaktioner på grund af sin carbonylgruppe og det aktive hydrogen, der støder op til carbonylgruppen. Kondensation forekommer ved opvarmning med saltsyre eller natriumhydroxid for at producere 3,4-dimethyl-3-hexen-2-on eller 3-methyl-3-hepten-5-on. Ved længere tids udsættelse for sollys produceres ethan, eddikesyre og kondensationsprodukter. Ved oxidation med salpetersyre dannes diacetyl. Ved oxidation med stærke oxidationsmidler såsom chromsyre genereres eddikesyre. Butanon er relativt stabil over for varme, og termisk spaltning ved højere temperaturer producerer enon eller methylenon. Ved kondensation med alifatiske eller aromatiske aldehyder produceres ketoner med høj molekylvægt, cykliske forbindelser, ketonkondensation og harpikser. For eksempel producerer kondensation med formaldehyd i nærvær af natriumhydroxid først 2-methyl-1-butanol-3-on, efterfulgt af dehydrering til methacrylaton.
Resinisering sker ved udsættelse for sollys eller UV-lys. Kondensation med phenol giver 2,2-bis(4-hydroxyphenyl)butan. Reagerer med alifatiske estere i nærvær af en basisk katalysator for at producere β-diketoner. Acylering med surt anhydrid i nærvær af en sur katalysator for at danne β-diketoner. Reagerer med hydrogencyanid for at danne cyanohydrin. Reagerer med ammoniak for at danne ketopiperidinderivater. α-hydrogenatomet i butanon kan let substitueres med halogener for at danne forskellige halogenerede ketoner, såsom 3-chlor-2-butanon, ved interaktion med chlor. Interaktion med 2,4-dinitrophenylhydrazin producerer gul 2,4-dinitrophenylhydrazon.
Anvendelse:
Methylethylketon (2-butanon, ethylmethylketon, methylacetone) er et organisk opløsningsmiddel med relativt lav toksicitet, som findes i mange anvendelser. Det bruges i industrielle og kommercielle produkter som opløsningsmiddel til klæbemidler, maling og rengøringsmidler og som afvoksningsmiddel. Methylethylketon, der er en naturlig bestanddel af nogle fødevarer, kan frigives til miljøet af vulkaner og skovbrande. Det bruges til fremstilling af røgfrit pulver og farveløse syntetiske harpikser, som opløsningsmiddel og i overfladebelægninger. Det bruges også som smagsstof i fødevarer.
MEK bruges som opløsningsmiddel til forskellige belægningssystemer, for eksempel vinyl, klæbemidler, nitrocellulose og akrylbelægninger. Det bruges i malingfjernere, lakker, fernisser, spraymaling, forseglere, lim, magnetbånd, trykfarver, harpikser, harpikser, rengøringsopløsninger og til polymerisering. Det findes i andre forbrugerprodukter, for eksempel husholdnings- og hobbycement og træfyldningsprodukter. MEK bruges til afvoksning af smøreolier, affedtning af metaller, i produktionen af syntetisk læder, transparent papir og aluminiumsfolie samt som et kemisk mellemprodukt og katalysator. Det er et ekstraktionsopløsningsmiddel i forarbejdningen af fødevarer og fødevareingredienser. MEK kan også bruges til at sterilisere kirurgisk og dentalt udstyr.
Ud over fremstillingen omfatter miljøkilder til MEK udstødning fra jet- og forbrændingsmotorer samt industrielle aktiviteter såsom forgasning af kul. Det findes i betydelige mængder i tobaksrøg. MEK produceres biologisk og er blevet identificeret som et produkt af mikrobiel metabolisme. Det er også blevet fundet i planter, insektferomoner og dyrevæv, og MEK er sandsynligvis et mindre produkt af normal pattedyrs metabolisme. Det er stabilt under almindelige forhold, men kan danne peroxider ved længere tids opbevaring; disse kan være eksplosive.
Produktkategorier
-

Telefon
-

E-mail
-

WhatsApp
-

Top













